一、什么是UDI?
唯一器械标识(Unique Device Identification,缩写UDI)是美国FDA建立的“特殊医疗器械识别系统”。对医疗器械在其整个生命周期赋予的身份标识,是其在产品供应链中的唯一“身份证”。
全球采用统一的、标准的UDI有利于提高供应链透明度和运作效率;有利于降低运营成本;有利于实现信息共享与交换;有利于不良事件的监控和问题产品召回,提高医疗服务质量,保障患者安全。
其中,UDI又包含着UDI-DI和UDI-PI。
UDI-DI。国际上通常表示为device identifier,即产品标识。是用于某种特定的规格型号和包装医疗器械的唯一代码。
产品标识(UDI-DI)可作为医疗器械唯一标识数据库存储信息的“访问关键字”,关联医疗器械产品信息、制造商信息、 注册信息等。
UDI-PI国际上通常表示为production identifier,即生产标识。是用于识别医疗器械生产过程相关数据的代码。
其中,生产标识(UDI-PI)可根据实际应用需求,含括医疗器械序列号、生产批号、生产日期、失效日期等信息。
目前,全球众多发达国家以及发展中国家都已经制定成熟的UDI政策法规,强制要求在本国销售、流通的医疗器械上必须实施UDI标识。
二、UDI码编码规则
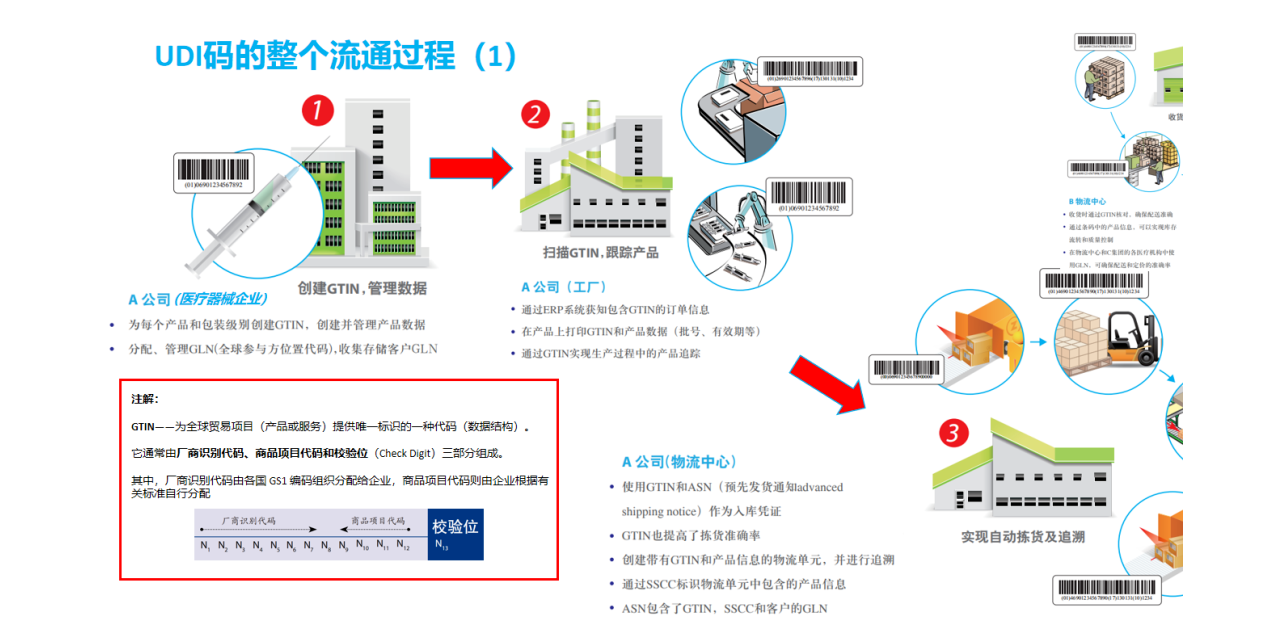
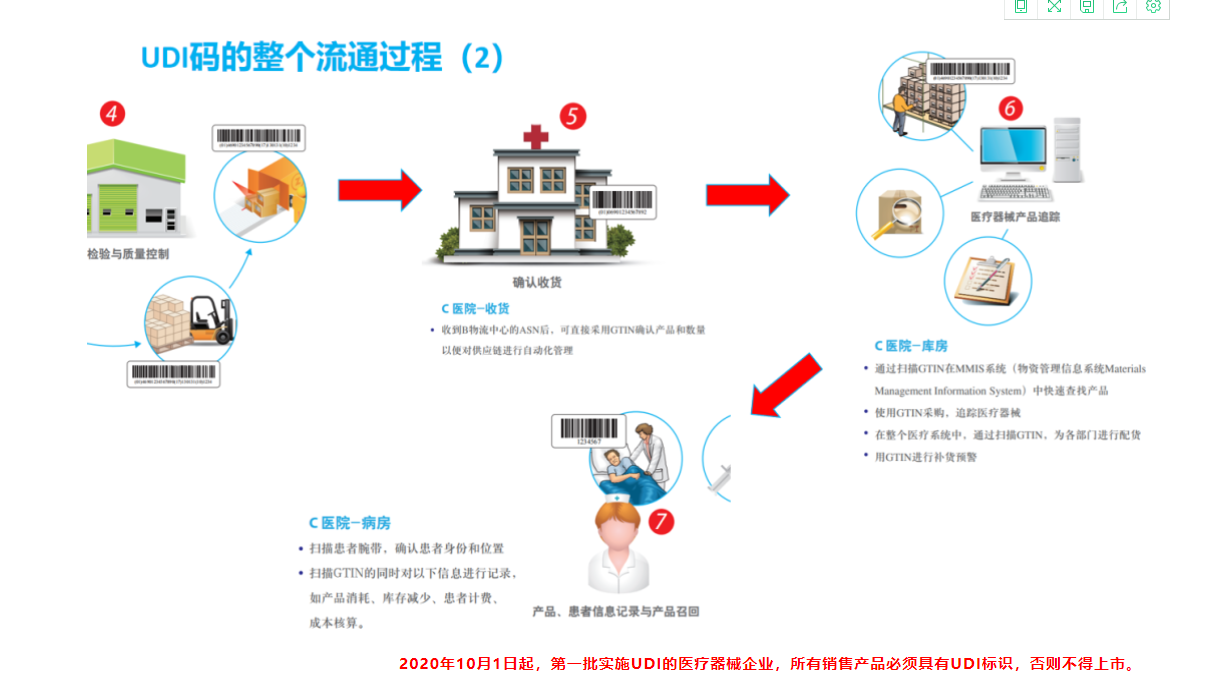
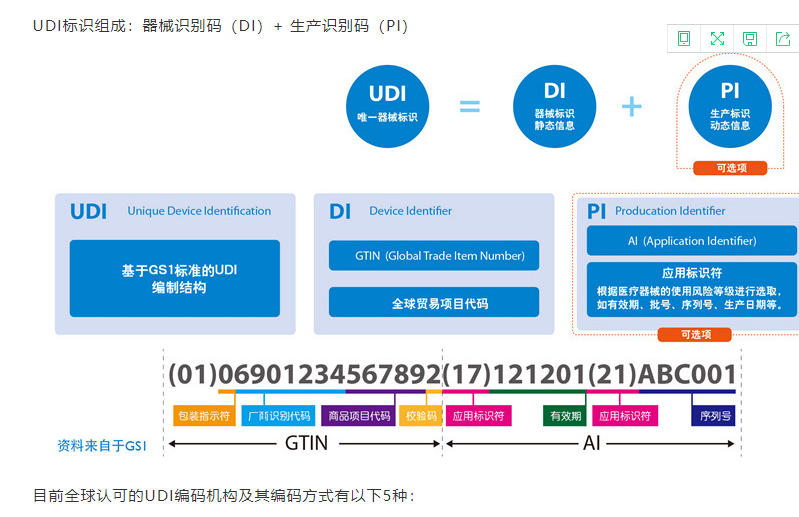
医疗器械唯一标识由产品标识(DI)和生产标识(PI)组成,产品标识(DI)是识别注册人/备案人、医疗器械型号规格和包装的唯一代码,是从数据库获取医疗器械相关信息的“关键字”,是唯一标识的必需部分;生产标识(PI)包括与生产过程相关的信息,包括产品批号、序列号、生产日期和失效日期等,可与产品标识联合使用,满足医疗器械流通和使用环节精细化识别和记录的需求。
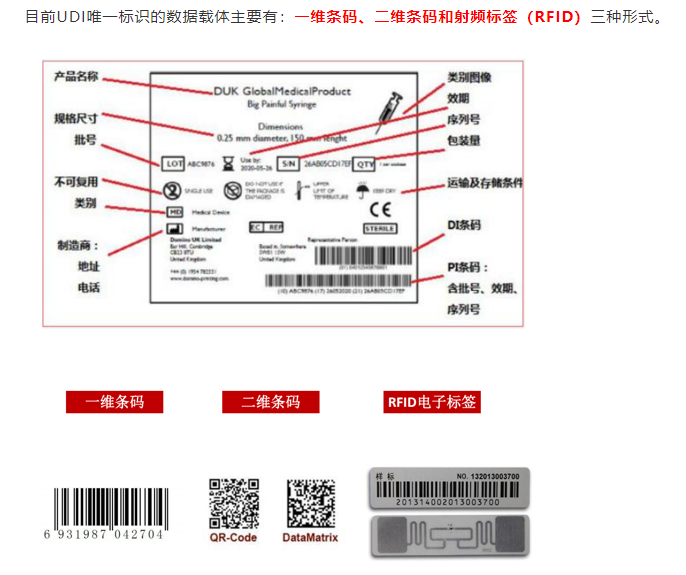
基于GS1标准的UDI编制结构,包括器械标识静态信息DI、生产标识动态信息PI。其中,DI包括全球贸易项目代码GTIN,具体有包装指示符、厂商识别代码、商品项目代码、校验码等。PI具体包括应用标识符、有效期、序列号、生产日期等。由于医疗器械使用风险和监管追溯要求的不同,其器械的唯一标识也会随之变化。UDI可由DI单独表示,也可由DI加PI联合使用表示。根据不同的医疗器械产品,可标识到规格型号、批次、单品。
三、UDI码赋码实施全过程
1、对接注册申请:登录国家UDI数据平台(https://udi.nmpa.gov.cn/),根据指引完成对接注册申请;
2、选择发码机构:医疗器械注册/备案人,选择有资质的发码机构;
3、UDI代码申请:医疗器械注册/备案人,根据发码机构指引完成UDI代码申请;
4、UDI标识赋码:医疗器械注册/备案人,采用喷码设备对产品进行赋码,为其赋予唯一身份标识;
5、UDI产品追溯:利用UDI码进行追溯管理,有利于不良事件的监控和问题产品召回,提高医疗质量,保障患者安全。
提示:每一台工控平台会生成不同的UDI码,所有产品UDI码都是现场生成,由现场工控平台上传至UDI追溯后台。
四、UDI医疗器械标识应用范围
第一批需要实现UDI管控的医疗器械有9大类器械分别包含:
01、有源手术器械
02、无源手术器械
03、神经和心血管手术器械
06、医用成像器械
10、输血、透析和体外循环器械
12、有源植入器械
13、无源植入器械
14、注输、护理和防护器械
16、眼科器械
五、UDI标识结构组成、编码机构、数据库
六 医疗器械实施UDI的好处
1、能简化将器械使用信息集成到数据系统的操作;
2、能快速识别出现不良事件的医疗器械;
3、能更快速地为已报告的问题制定对应解决方案;
4、能够减少医疗事故发生;
5、提供更迅速、有效的器械召回数据;
6、实现突出重点且有效的药监部门安全沟通;
7、可以轻松访问准确器械标识信息的原始来源。
Copyright © 2020 武汉先同科技股份有限公司 All Rights Reserved. 鄂ICP备15021610号-1